Les substances sémiochimiques :
Les substances sémiochimiques sont des molécules organiques synthétisées par un organisme vivant et qui interviennent comme moyen de communication que ce soit de manière intraspécifique ou de manière interspécifique. Ces substances sémiochimiques modifie le comportement ou la physiologie du récepteur.
Les actions interspécifiques, ont lieu grâce aux substances allélochimiques, ce sont des actions concernant les relations entre différentes espèces alors que les actions intraspécifiques, ayant lieu grâce aux phéromones sont relatifs aux rapports qui se produisent au sein d’une même espèce.
Nous allons nous intéresser aux phéromones pour étudier la communication chimique qui a lieu au sein d’une même espèce : les fourmis.
Définition de phéromone:
La notion de phéromone a été introduite par Karlson et Lüsher en 1959, ils en ont donné la définition suivante : « Une phéromone est une substance (ou un mélange de substances) qui, après avoir été sécrétée à l’extérieur par un individu (émetteur), est perçue par un individu de la même espèce (récepteur) chez lequel elle provoque une réaction comportementale spécifique, voire une modification physiologique ». Le mot phéromone vient du grec pherein « transporter » et hormân « exciter ». Les phéromones sont produites par des glandes spécifiques et sont secrétées à l’extérieur d’un organisme. Comme les enzymes, elles agissent dans des quantités minimes. Nous allons étudier un peu plus tard ces glandes spécifiques dans la partie émission.
Généralement, on ne parle pas d’une seule phéromone mais plutôt d’un bouquet phéromonale. En effet, les phéromones ne sont pas des corps purs mais des mélanges de différentes substances chimiques. Le message transmis est spécifique, déterminé par sa composition qualitative et quantitative.
Les différents types de phéromones :
Le célèbre scientifique Wilson, en 1962, distingue les phéromones de déclenchement aux phéromones modificatrices selon leurs modes d’action. Selon lui :
-
« Les phéromones de déclenchement produisent un changement d’état immédiat et réversible dans le comportement du récepteur ». Il y classe les phéromones sexuelles (attractives ou aphrodisiaques), les phéromones d’alarme, les phéromones de piste, les phéromones d’agrégation, les phéromones de territoire…
-
« Les phéromones modificatrices élaborent une suite de modifications physiologiques chez le récepteur, sans aucun changement immédiat dans son comportement ». cependant, ces modifications physiologiques lui permettent ultérieurement d’acquérir un nouveau répertoire comportemental, pouvant se manifester suite à une situation donnée. De plus, ces phéromones réagissent dans le déterminisme des castes chez les insectes sociaux comme les fourmis ou les abeilles. En effet, Wilson décrit que la reine peut créer une « substance royale » qui développe les ovaires des ouvrières.
Dans ces deux catégories, on distingue différents types de phéromones. Nous allons maintenant nous intéresser aux différentes phéromones de déclenchement car ce sont les phéromones les plus étudiées par les scientifiques :
-
phéromones de territoire : utilisées pour marquer le territoire et pour le repérer, il s’agit de phéromones utilisées par certains mammifères comme les chats ou les chiens mais aussi par les poissons. On les retrouve dans les urines. En ce qui concerne les fourmis, les phéromones territoriales assure la sécurité de la fourmilière. Ainsi, elles sont déposées pour marquer l’abord du nid. Elles sont secrétées par la glande de Dufour. Elle exerce deux rôles principaux. Premièrement, elle permet aux ouvrières de la fourmilière de se repérer pour rejoindre leur nid. Et enfin, elle porte une action répulsive envers les fourmis d’autres colonies.
-
phéromones d’alarme : comme leur noms l’indique, ces phéromones utilisées par les insectes, les poissons, et mammifères permettent aux animaux d’alerter d’un danger. Chez les fourmis, on constate que la réaction agit de façon collective. En effet, dès lors qu’une fourmi sécrète une phéromone d’alarme, les autres fourmis présentent réagissent et sécrètent à leurs tours cette même phéromone ainsi la réaction devenant collective permet de mieux contrôler les dangers. On en conclut alors que le rôle premier de ces substances chimiques est d’avertir les autres congénères de la fourmilière d’un danger. Selon BLUM et PASSERA, « ces phéromones constituent un progrès dans l’évolution des espèces eusociales ». Les jets d’acide formique, tirées à plusieurs centimètres par les fourmis, sont un exemple de ce phénomène

Photo illustrant les jets d’acide formique
Le comportement d’alarme peut-être divisé en deux activités. Tout d’abord, on constate « un mouvement de panique », ainsi les différentes fourmis adoptent un comportement agressif auquel s’ajoute un déplacement à grande vitesse vers le danger. Puis, les fourmis adoptent une attitude d’attaque, elles ouvrent leurs mandibules et attaquent l’insecte dangereux en piquant pour déposer du venin.
Comme nous allons l’aborder plus tard, il faut noter que les phéromones d’alarme sont secrétées par les glandes mandibulaire, la glande de Dufour, ou encore la glande à poison.
Généralement, ces substances chimiques forment des chaînes carbonées plus courtes que celle des phéromones d’alarmes comme nous le montrent ces exemples dans les tableaux suivants. C’est pourquoi, elles sont plus volatiles et ainsi elles possèdent une durée de vie courte. Ces phéromones d’alarme sont souvent des cétones (comme l’octan-2-one que nous avons synthétisé, voir partie utilisation de ces connaissances par l’homme), des esters, des alcools, des hydrocarbures comme l’exemple du décane.
Différentes phéromones d’alarme sont utilisées par les mêmes espèces. Elles sont donc moins spécifiques que les phéromones de piste, ainsi l’acide formique est non seulement utilisé par les formicas rufa (fourmis des bois) mais aussi par les Camponotus.
Chez certaines espèces, on a pu tracer différents cercles démontrant les champs d’action des phéromones. Par exemple, la fourmi tisserande d’Afrique Oecophyllalonginoda secrète grâce à ses glandes mandibulaires quatre substances principales qui agissent dans un périmètre particulier. En voici, le schéma :
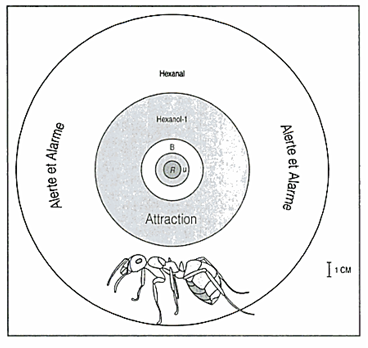
Phéromones d’alarme : comportement d’une ouvrière tisserande Oecophyllalonginodo alarmée par une glande mandibulaire écrasée au centre du dispositif circulaire. Les diverses phéromones d’alarme sont plus au moins volatiles et déclenchent des comportements différents. B : 2-butyl-2-octénal, U : 3-undécanone, R : répulsion (modifié d’après Bradshaw)
L’hexanal, composé organique de la famille des aldéhydes, est la substance chimique la plus volatile, elle déclenche un état d’alerte chez les fourmis se trouvant à une dizaine de centimètre de la source qui a été mordue. Lorsque les fourmis ouvrières s’approchent et se trouvent à cinq centimètres, elles sont attirées par le centre mais le 1-hexanol, substance chimique qualifiable de « lourde » agit comme répulsif, cependant son temps de vie est limité. Cette action répulsive permet d’attirer plus de fourmis dans le cercle afin de permettre à un ensemble de fourmis de s’attaquer collectivement et efficacement. Peu à peu, l’effet répulsif diminue par évaporation. Ainsi, le 3-undécanone et le 2-butyl-2-oclénal se trouvant au centre du dispositif sont les substances chimiques les plus « lourdes », elles permettent de déclencher un comportement de morsure
Exemple de phéromones de piste que nous avons modélisées grâce au logiciel ChemSketch, il faut noter que ce logiciel ne prend pas en compte les liaisons doubles :
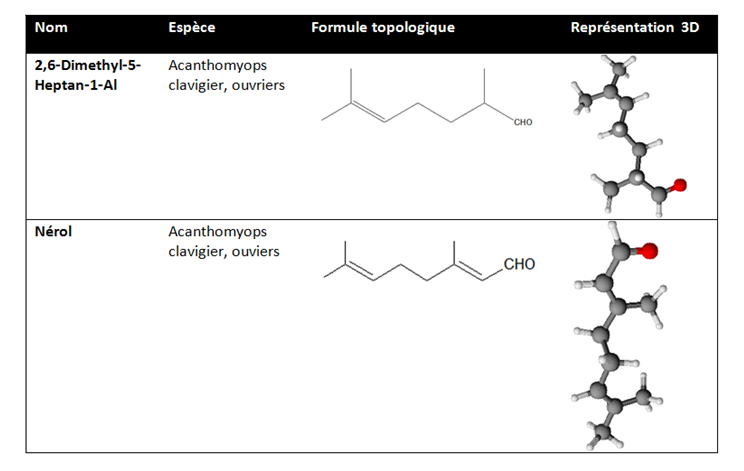
- Les phéromones de piste : Utilisées par les insectes sociaux ainsi que les mammifères, ces phéromones permettent de tracer une piste chimique. Elles sont à l’origine d’un recrutement d’autres fourmis. Elles sont utilisées pour l’approvisionnement de nourriture à la fourmilière mais aussi pour neutraliser un ennemi ou pour le déménagement à un nouveau nid. Pour réaliser cette piste chimique, la fourmi secrète la phéromone en frottant son aiguillon ou l’extrémité de son abdomen sur le sol. Cette méthode permet l’augmentation progressive du nombre de fourmis recrutées.
Les chercheurs ont démontré qu’il existe au moins neuf glandes permettant la sécrétion de phéromones de piste. La plupart de ces phéromones se trouvent dans l’abdomen par exemple dans la glande de Dufour ou dans les glandes à poison.
Nous pouvons réaliser une expérience permettant de démontrer l’utilisation d’une piste chimique : prenons une fourmi qui va de la fourmilière vers une source de nourriture. La première fourmi va secréter une phéromone qui « traversera son chemin » de retour à sa fourmilière. Les autres fourmis sont alertées et suivront la même piste qu’a suivie la première fourmi pour apporter de la nourriture à la fourmilière.
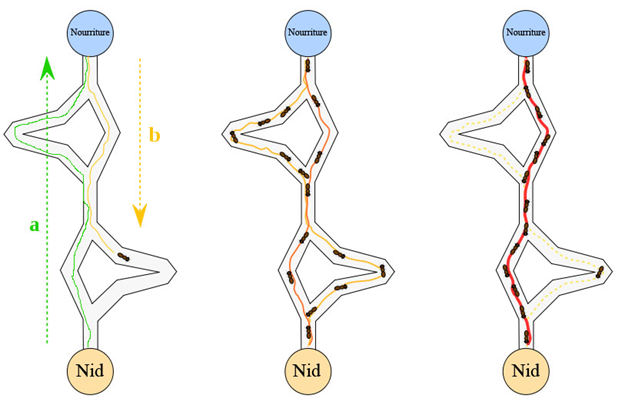
Schéma des parcours utilisé lors des expériences et observation de différents moments
On constate que plus les fourmis font des aller- retour, plus elles ont tendance à emprunter le chemin le plus court. Ainsi, le bouquet phéromone des phéromones de piste permet aux fourmis de marquer un « trajet » qu’elles signalent à d’autres fourmis. De plus, les substances secrétées permettent aussi aux autre fourmis de connaître la quantité de nourriture disponible, à leur tour elles sécrèteront ce bouquet tant que la nourriture est disponible.
Voici deux exemples de phéromones de piste :
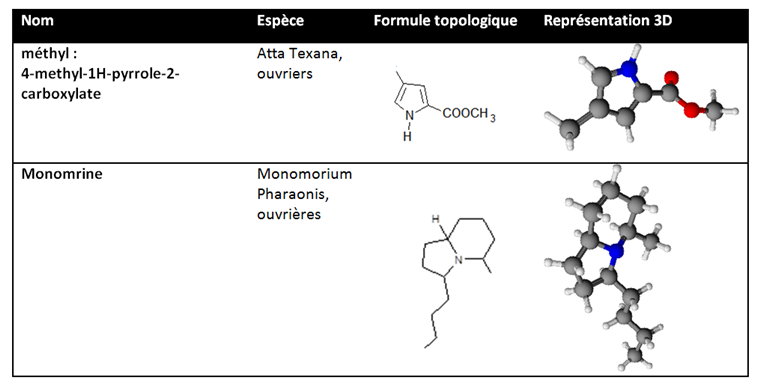
On doit ajouter à cela que les scientifiques Regnier et Wilson ont calculé l’efficacité de la perception des phéromones d’alarme chez certaines espèces. Ainsi, les Acanthomyops claviger perçoivent les phéromones d’alarme dès lors que la concentration atteint 1010 à 1012 molécules/cm3. Et chez les Atta Texana, l’efficacité est atteinte dès lors que la concentration est de 108 molécules/cm3.
- Les phéromones d’agrégation : Les phéromones d’agrégation sont un véritable outil chez les fourmis pour assurer la cohésion sociale. Ainsi, elles ont un rôle important pour la reproduction, pour l’hibernation, pour nidifier, pour estiver ou encore la protection sociale. Ces phéromones ont une durée de vie très variable les unes des autres. En effet, elles peuvent agir temporairement ou de façon permanente pour assurer la cohésion sociale. Voici un exemple de phéromones d’agrégation, il s’agit d’une phéromone spécifique des Coléoptères. En effet, il existe très peu d’étude concernant les phéromones d’agrégation des fourmis.
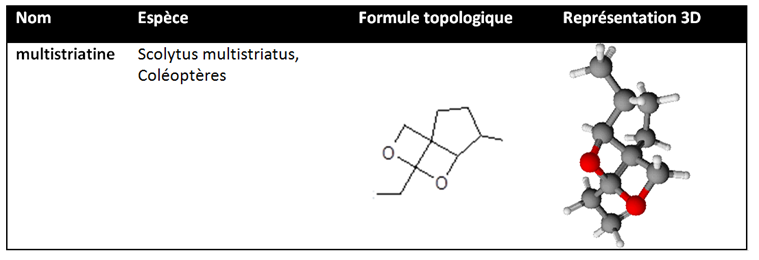
- Les phéromones passeports : elles sont comparables à une « carte d’identité » de la fourmi. Ainsi, elles sont imprégnées sur leurs cuticules et permettent aux autres fourmis de les identifier par rapport à leur fourmilière à partir d’un contact antennaire. Ces phéromones sont certes des substances chimiques mais leurs modes de communication est tactile et non chimique c’est pour cela que nous n’allons pas les détailler. Cependant, on peut aussi considérer que le nid imprégné de phéromones passeport permet aux colonies de se reconnaître les unes par aux autres. Voici un exemple de phéromones passeport :
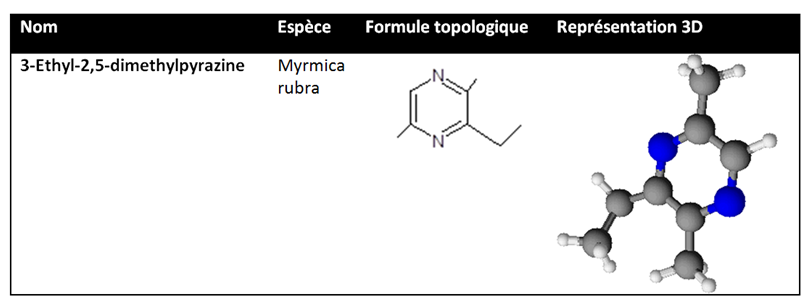
- Les phéromones sexuelles : Elément essentiel lors de la reproduction, les phéromones sexuelles permettent aux fourmis d’attirer les fourmis du sexe opposé. Il faut noter que ces phéromones sont la plupart du temps émises par les femelles afin d’attirer les mâles. Selon des études, la plupart des phéromones émises par les femelles sont des hydrocarbures. La longueur de la chaine carbonique moyenne est de dix à vingts atomes de carbone. Elles permettent aussi de connaître le sexe de l’individu. Ces phéromones sont de véritables signaux olfactifs présents chez de nombreux insectes.
On distingue deux catégories de phéromones sexuelles :
-
Les substances d’appels secrétés par des glandes en dehors de l’appareil génital.
-
Les substances aphrodisiaques qui entrainent l’accouplement. C’est le cas de certains alcaloïdes.
Voici un exemple de phéromone sexuelle qui est une cétone :
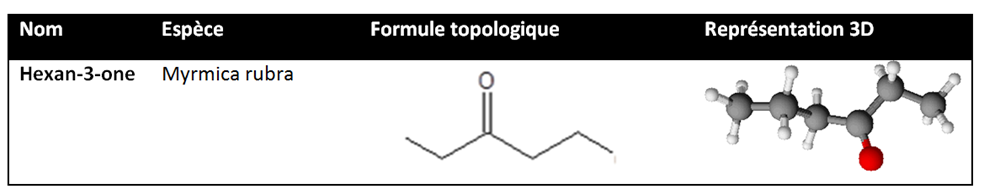
- Les phéromones de recrutement : elles permettent de recruter d’autres fourmis afin de donner une aide. Elles provoquent un regroupement de plusieurs fourmis en un point précis. Elles sont utilisées par exemple pour l’approvisionnement en nourriture. Elles sont un enchaînement des phéromones de piste. Ces phéromones sont aussi utilisées lors d’un déménagement d’un nid à l’autre. Il faut noter que les phéromones d’alarme provoquent aussi un regroupement mais celui-ci est défensif, de plus ce n’est pas le rôle premier des phéromones d’alarme. C’est pour cela qu’il ne faut pas les confondre avec les phéromones de recrutement.
Synthèse des différents types de phéromones utilisés dans la communication chimique des fourmis :
Toutes les phéromones que nous avons citées précédemment sont des molécules organiques car elles possèdent principalement les éléments carbone et hydrogène. Généralement, la longueur de la chaine carbonée témoigne de l’efficacité de la molécule. Certaines phéromones sont spécifiques de l’espèce (c’est le cas de la phéromone d’agrégation des coléoptères) mais elles sont dans d’autre cas utilisées par plusieurs insectes. D’autre part, certaines phéromones sont utilisées dans le même but comme par exemple la phéromone de piste et les phéromones de recrutement lors de l’approvisionnement en nourriture. Le message émis par les fourmis ne résulte pas d’une seule phéromone mais de différents types de phéromones constituants le bouquet phéromonal.
Emission des phéromones
Synthèse et transport des phéromones
Les fourmis produisent des messagers chimiques par le biais de cellules sécrétrices dont l’ensemble forme des glandes. Ces messages chimiques se répandent dans l’environnement. En effet, il s’agit de substances chimiques volatiles : des phéromones qui possèdent une durée de vie limitée. Il faut noter que l’effet de phéromone résulte de la taille de la molécule. En outre, on constate que plus la durée d’action de la molécule est longue plus la molécule est grande.
Ces substances chimiques sont synthétisées par une fourmi émettrice afin de transmettre une information à une fourmi réceptrice. Ainsi, ces phéromones peuvent être transmises par le transport de l’air, le placement au sol, et par contact.
La structure des glandes exocrine et les différents types de glandes.
Structure des glandes exocrines
Définition : Une glande exocrine est un organe sécrétant des substances chimiques. Dans notre cas, il s’agit des phéromones, qui sont rejetées à l’extérieur de l’organisme des fourmis. De plus, ces glandes ont aussi pour rôle de synthétiser les phéromones qu’elles sécrètent.
Il existe au moins trois types de glandes exocrines pouvant être distinguées selon le tableau suivant :

Nous pouvons voir la structure de ces glandes grâce au schéma ci-dessous et ainsi étudier l’évacuation des phéromones.
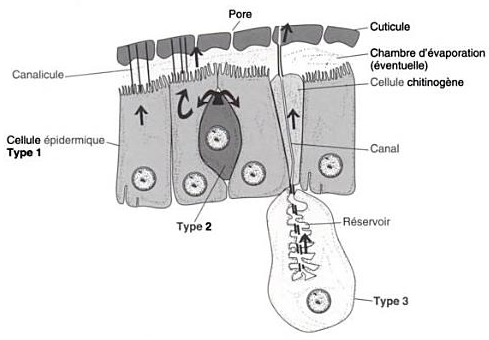
Schéma de la structure des glandes à phéromones chez les insectes, selon Brossut, 1996
L’évacuation des phéromones dépend des différents pores de la glande. Selon le type de cellules où se trouve la phéromone, l’évacuation est différente. Pour les cellules de types 1 : cellules glandulaire épidermique, la phéromone est rejetée par des canaux très étroits qui se situent dans la cuticule. En ce qui concerne les cellules de type 2 : les cellules glandulaires intra-épidermique, la phéromone est évacuée par des canaux fins ou par les chambres d’évacuation suite à leurs transports par les cellules adjacentes. Enfin, les cellules de type 3 : les cellules sous-épidermique, la phéromone est rejetée par un réservoir central grâce à un canal cuticulaire.
Les différentes glandes exocrines
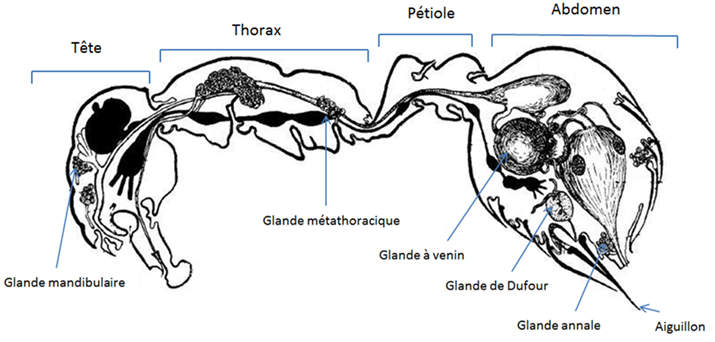
Schéma du système glandulaire de la fourmi
-
Glande mandibulaire : Située en dessous des mandibules, la glande mandibulaire synthétise les phéromones d’alarme. Elle produise aussi un liquide peu fluide qui permet de malaxer et de ramollir la nourriture retrouvée par les fourmis. Ces substances chimiques sont principalement constituées de citronellol et de citronellal qui ont respectivement une fonction défensive et déclencheur d’alarme. D’autre part, ces glandes mandibulaires permettent le maintien de la hiérarchie sociale.
-
Glande métathoracique : elle produit des substances chimiques qui contribuent sans doute au repérage ou à la défense.
-
Glande Anale : elle contient principalement des esters volatiles. Ces glandes produisent l’acide formique qui est une substance chimique défensive. Cet acide peut être projeté à plusieurs centimètres.
-
Glandes pygidiale : elle produit des phéromones d’alarme et permet ainsi d’alerter les autres fourmis.
-
Glande de Dufour ou alcaline : surnommée le « flacon à parfum » des fourmis. Il s’agit d’une phéromone de piste, qui est le moyen de recruter les congénères, grâce au traçage d’une piste chimique. Cette substance chimique est active durant 100 secondes. Ces phéromones sont ensuite rejetées par l’aiguillon.
-
Glande à poison ou à venin : comme la glande anale, elle produit de l’acide formique, il s’agit donc d’une glande qui synthétise des phéromones d’alarme qu’elle utilise face à un danger. Cette glande, chez certaines espèces, rejette du venin qui a un rôle paralysant, d’où son nom. Ces substances chimiques sont ensuite secrétées par l’aiguillon.
Réception d’un signal chimique : les antennes, des récepteurs sensoriels
Chez la fourmi, comme tous les autres insectes, la réception des signaux chimiques se fait par le biais de récepteurs sensoriels. Ces chimiorécepteurs sont des cellules sensorielles spécialisées qui se situent au niveau des organes olfactifs c’est-à-dire les antennes.
Les fourmis possèdent toutes, deux antennes constituées de cellules sensorielles. Elles sont observables au microscope optique à balayage.
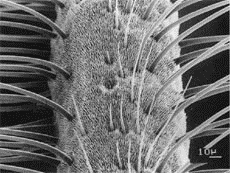
Nous observons ainsi que les antennes sont constituées de cils. En effet, il s’agit de sensilles. Chaque sensille réagit à une phéromone ou un bouquet phéromones. Lorsque nous observons de plus près ces sensilles, on remarque qu’ils sont constitués de plusieurs pores qui permettent la traversée des phéromones.
Les sensilles sont constituées de dendrites. Il s’agit de neurones sensoriels qui permettent la réception et la transmission d’un signal chimique auparavant qui se transforme en signal électrique aux corps nerveux composés de cellules sensorielles. Il faut noter qu’une sensille peut contenir de 2 à 5 neurones olfactifs. Les cellules sensorielles sont reliées à l’axone qui permet de transférer le message électrique au cerveau des fourmis qui l’analyse pour obtenir des informations concernant une source alimentaire retrouvée par une fourmi (la qualité, ou la quantité).
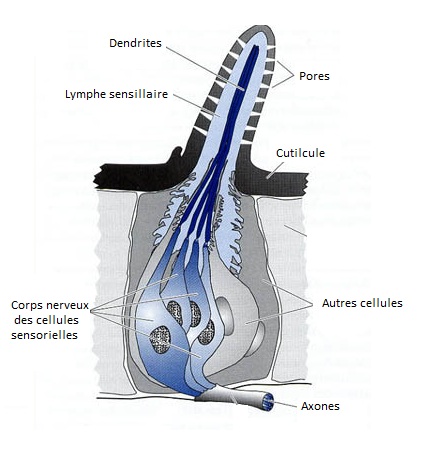
Schéma de la structure d’une sensille
On trouve, au niveau des dendrites, des récepteurs olfactifs permettant l’identification du stimulus (éléments extérieurs capables de déclencher des phénomènes spéciaux dans l’organisme : odeur, phéromones). Les récepteurs olfactifs se composent d’une protéine et d’un glucide qui forment un site actif auquel se fixe la molécule (la ou les phéromone(s)). Ainsi les récepteurs olfactifs sont spécifiques d’une molécule ou plusieurs molécules (pour les bouquets phéromonaux). En effet, les phéromones sont transportées dans le liquide sensillaire grâce aux OBP (olfactorybindingproteins) et les PBP (pheromonebindingprotein), qui sont des protéines spécifiques. La molécule odorante est ensuite perçue par l’odorant receptorprotein (Or) afin d’être transmise par les dendrites au corps nerveux des cellules sensorielles.
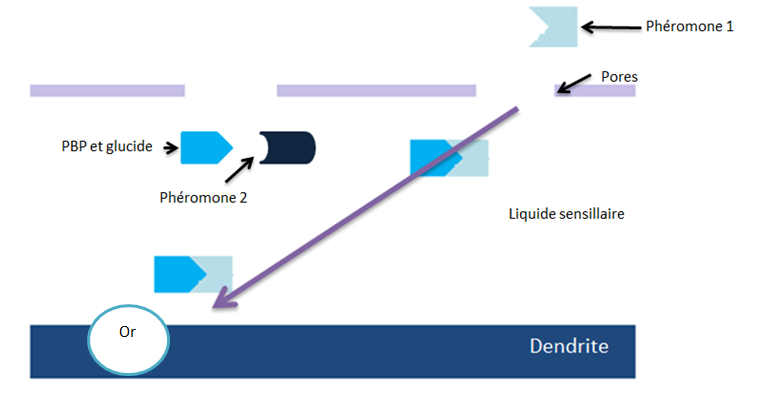
Schéma de la réception des phéromones au niveau du liquide sensillaire
Utilisation de ces connaissances par l’homme
Synthèse d’une phéromone par l’homme
Afin de se servir de ces connaissances en matière de communication chimique, l’homme doit copier le système de communication chimique c’est-à-dire les phéromones, en les synthétisant. On doit étudier précisément la composition phéromonale des glandes, afin de synthétiser une phéromone laboratoire comme par exemple l’octan-2-one. Les synthèses des phéromones permettent à l’homme de les utiliser en tant qu’outil contre la destruction culturale comme nous allons le voir un peu plus tard. Nous avons donc procédé à une expérience afin de synthétiser l’octan-2-one, une phéromone, grâce à l’octan-2-ol. Cette phéromone se trouve dans les glandes mandibulaires des fourmis. Voici les représentations du réactif principal et du produit.
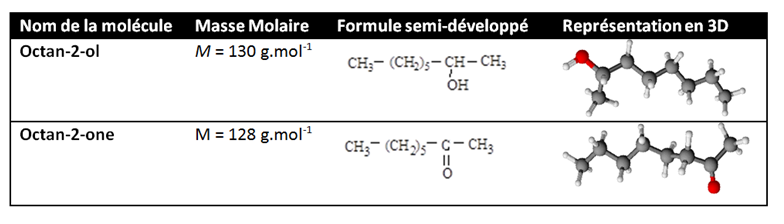
Nous avons donc suivi un protocole expérimental réalisé par un enseignant de l’académie de Nantes que nous avons modifié afin de répondre au mieux aux contraintes de matériel de laboratoire.
1. Mise en place des réactifs et déroulement de la transformation chimique :
Introduire dans le ballon le turbulent et, à l’aide d’éprouvettes graduées, sous la hotte :
5 mL d’octan-2-ol,
10 mL d’acide éthanoïque .
Mettre l’agitateur magnétique en fonctionnement.
Suivre la diminution de la température jusqu’à 15°C avec un thermomètre, avant de placer l’ensemble bouchon + tulipe + tube.
Introduire dans l’ampoule de coulée isobare 40mL d’eau de javel à 24 °chl.
Afin de doser la concentration de l’eau de javel à 24 °chl comme le recommande le protocole, nous avons étudié la définition du degré chlorométrique. Ainsi, le degré chlorométrique d est le nombre de litres de dichlore gazeux Cl2, pris dans les conditions normales de température et de pression, qu’il faut dissoudre dans un litre d’une solution d’hydroxyde de sodium pour obtenir un litre d’eau de javel titrant d °chl, selon la réaction :
Cl2(g) + 2Na+ + 2OH– → 2 Na+ + ClO– + Cl– + H2O
Dans des conditions de pression et de température normales on doit dissoudre 24L de dichlore gazeux dans 1L de soude afin d’obtenir 1L d’eau de Javel.

Photo du montage expérimental que nous avons réalisé, l’ampoule de coulée isobare n’a pas été encore introduite
Lorsque la température est inférieure à 15°C, faire couler l’eau de javel goutte à goutte en veillant à ne pas dépasser la température de 25°C. L’addition doit être lente (au goutte à goutte).
Lorsque l’ampoule de coulée est vide, enlever le cristallisoir et laisser revenir à la température ambiante tout en agitant pendant 15 minutes. Enlever l’ampoule de coulée et la rincer.
La solution doit rester de couleur jaunâtre ce qui prouve que l’eau de javel est en excès par rapport à l’octan-2-ol. Si l’eau de javel n’est pas en excès, ajouter quelques mL d’eau de javel dans le mélange réactionnel.
En fin de synthèse, remettre l’ampoule de coulée en place et y placer environ 5mL d’une solution d’hydrogénosulfite de sodium (Na+ + HSO3–). Faire couler goutte à goutte la solution d’hydrogénosulfite de sodium dans le mélange réactionnel jusqu’à décoloration totale de la solution

Photo du montage lorsque l’eau de Javel coule en goutte à goutte

Photo de l’eau de la solution d’hydrogénosulfite de sodium qui coule doucement, la solution auparavant jaune est devenue incolore
2. Lavages de la phase organique :
Récupérer le turbulent. Transvaser le contenu du ballon à l’aide d’un entonnoir dans une ampoule à décanter, rincer le ballon avec 20mL d’eau distillée froide et récupérer cette eau de lavage dans l’ampoule à décanter.
Ajouter dans l’ampoule à décanter 50mL d’une solution aqueuse de chlorure de sodium saturée préalablement refroidie dans le bain eau + glace pilée.
Agiter l’ampoule à décanter et laisser reposer quelques minutes afin de séparer la phase aqueuse et la phase organique. Eliminer la phase aqueuse. La phase organique est peu abondante.
Laver la phase organique avec 50mL d’une solution d’hydrogénocarbonate de sodium à 5 %, solution préalablement refroidie dans le bain réfrigérant.
Attention au dégagement gazeux ! Lorsque celui-ci est atténué, agiter l’ampoule à décanter en dégazant l’ampoule plusieurs fois. Laisser reposer et éliminer la phase aqueuse.
Laver une dernière fois la phase organique avec 50mL d’une solution aqueuse de chlorure de sodium saturée, préalablement refroidie dans le bain réfrigérant. Eliminer la phase aqueuse et recueillir la phase organique dans un erlenmeyer propre.

Photo de l’ampoule à décanter lors du dernier lavage de la phase organique avec 50ml d’une solution aqueuse de chlorure de sodium saturée, préalablement refroidie dans le bain réfrigérant
3. Séchage de la phase organique :
Sécher la phase organique avec un sel anhydre comme par exemple du sulfate de magnésium anhydre.

Photo du séchage de la phase organique avec du sel anydre
4. Filtrer la phase organique avec un dispositif de Büchner

Photo du dispositif de Büchner réalisé afin d’obtenir le produit
5. Caractérisation du groupe carbonyle de la cétone obtenue :
Dans un tube à essai, verser environ 2 mL de solution de D.N.P.H. et y ajouter quelques gouttes d’octan-2-ol. Agiter le tube à essai et observer.
Refaire la même opération avec quelques gouttes du liquide organique obtenu au cours de cette synthèse.

Photo du tube à essai contenant le liquide organique, ajout de quelques gouttes de DNPH
La synthèse enfin terminée, nous pouvons donner l’équation de la réaction d’oxydoréduction lors de cette transformation chimique :
ClOH + H+(aq) + 2 e– = Cl– + H2O
C8H18O = C8H16O + 2 H+(aq) + 2 e–
C8H18O + ClOH → C8H16O + H+(aq) + Cl– + H2O
Grâce à un tableau d’avancement ci-dessous nous pouvons calculer le rendement maximum de la synthèse de l’octan-2-ol.
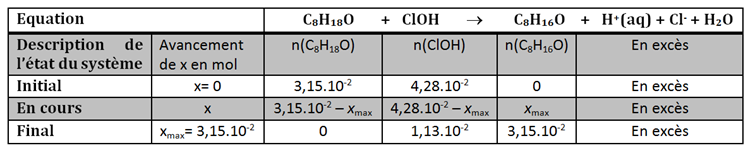
Quelque calcul afin de remplir le tableau :
m(C8H16O) = V(C8H16O) × d(C8H16O) × ρeau
m(C8H16O) = 5.0 × 0,819 × 1.00 = 4,1 g
Lutte intégrée
Depuis de nombreuses années, l’agriculture repose sur l’utilisation de pesticides afin de lutter contre les insectes ravageurs. Pourtant, d’autres solutions plus respectueuses de l’environnement existent. Il s’agit de la lutte intégrée. Elle a été définie au plan européen comme « l’application rationnelle d’une combinaison de mesures biologiques, biotechnologiques, chimiques, physiques, culturales ou intéressant la sélection des végétaux dans laquelle l’emploi de produits chimiques phytopharmaceutiques est limité au strict nécessaire pour maintenir la présence des organismes nuisibles en dessous de seuil à partir duquel apparaissent des dommages ou une perte économiquement inacceptable. »
Nous allons donc nous intéresser aux mesures chimiques que l’homme peut appliquer. En effet, en étudiant les insectes ravageurs, l’homme peut en déduire les phéromones qu’utilisent ces derniers et il peut ainsi réaliser une synthèse de cette phéromone qui lui permettra d’éliminer ou de limiter la population du ravageur dans un territoire précis comme c’est le cas de la méthode de la confusion sexuelle qui est mise en pratique grâce à des moyens biotechniques afin d’utiliser la synthèse d’une phéromone, il s’agit des diffuseurs.
Les avantages des phéromones par rapport aux insecticides :
L’utilisation de phéromones est un enjeu majeur pour l’agriculture car elles présentent plusieurs avantages face à l’utilisation des insecticides. Tout d’abord, l’utilisation de la synthèse des phéromones permet de cibler l’action agricole, c’est-à-dire que l’utilisation des phéromones permet une sélectivité dans le contrôle des nuisibles, ce qui est impossible avec les insecticides. En effet, leurs effets se manifestent même pour des insectes utiles qui sont touchées par le traitement. Les phéromones ne détruisent pas l’équilibre biologique car le traitement ne vise qu’une seule espèce. De fait, le traitement est spécifique d’une seule espèce. D’autre part, les phéromones permettent de préserver la biodiversité mais aussi l’environnement alors que les insecticides agissent comme des poisons, ils ne sont pas spécifiques d’une espèce. Ils polluent ainsi l’environnement. En utilisant les phéromones, l’homme copie ce qu’utilisent les insectes pour communiquer, dans le but de limiter les ravages culturaux. L’avantage des phéromones réside donc aussi dans le fait qu’elles soient biodégradables. Les quantités nécessaires pour attirer un insecte sont d’environ 15g alors que l’utilisation des insecticides implique l’utilisation de quantités importantes. Il est donc plus avantageux d’utiliser des phéromones pour permettre au mieux la préservation de l’environnement.
Méthode de la confusion sexuelle
Afin de réduire la population cible (souvent des insectes), l’homme a recours à plusieurs méthodes comme celle de la confusion sexuelle. Il utilise ainsi les connaissances qu’il a accumulées concernant la communication chimique. Ainsi, il sait que les phéromones sexuelles sont à l’origine de la reproduction. L’homme utilise la méthode de la confusion sexuelle en libérant des phéromones sexuelles synthétisées en laboratoire. Il désoriente ainsi l’insecte en agissant sur les chimiorécepteurs de l’animal. Cette libération de phéromones engendre une fatigue sensorielle, ainsi, le mâle n’est plus capable de trouver les femelles. En effet, l’homme a camouflé les phéromones naturelles émises par les femelles. Il existe ainsi une confusion entre les phéromones d’origine naturelle et celles d’origine synthétique. Dès lors, cette méthode réduit le nombre total d’accouplement ou entraine un retard. Le taux de fécondité est par conséquent réduit ce qui provoque une diminution de la population cible sur l’espace où la phéromone sexuelle de synthèse a été diffusée.
Cette méthode de lutte chimique est généralement utilisée contre les micro-lépidoptères de la famille des tortricidés (tordeuses). Elle préserve ainsi les cultures tels que les vignobles, les cultures de pommes, ceux de cerises, de prunes et de maïs.
Le piégeage sélectif
On utilise par exemple la méthode du piégeage sélectif, du ravageur mâle ou de la femelle mais aussi des deux à la fois. Cette méthode est souvent utilisée pour un suivi du ravageur permettant de constater ou non leur présence. Elle permet aussi de donner une estimation sur les insectes ravageurs. C’est aussi un outil permettant de connaître la période de reproduction et d’estimer ainsi la période d’attaque. Voici quelques exemples de pièges utilisés en agriculture :
Les pièges à entonnoir et le pièges à ailette : une capsule permettant la diffusion de phéromones y est fixée. Chaque capsule est spécifique d’une seule espèce. Le récipient contient de l’eau afin que les insectes se noient. Les ravageurs souvent des lépidoptères sont attirés par la phéromone. Ils volent ainsi tous autour jusqu’à un épuisement total pour enfin tomber dans l’entonnoir. Ces pièges sont souvent destinés à des cultures de petite taille ou pour des jardins.
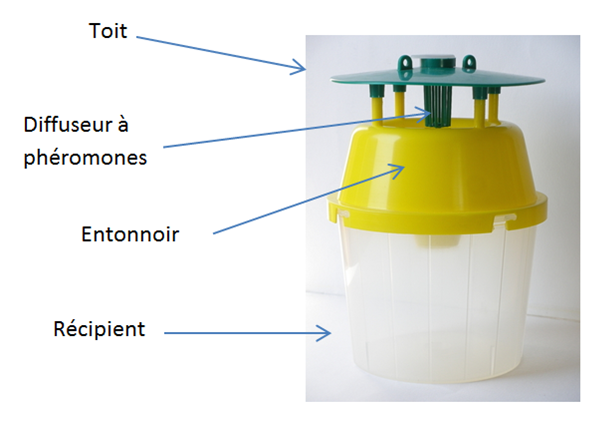
Les pièges Delta : Ils agissent sur le même principe que les pièges à entonnoir. Cependant les insectes tombent sur une plaque de glu. Ce type de piège est souvent utilisé afin de faire des statistiques sur les insectes ravageurs, de connaître la période de reproduction. Un quadrillage y est dessiné afin de faciliter le comptage.

Quel que soit le piège utilisé, l’agriculteur en changeant la capsule et les plaques collantes peut les réutiliser infiniment. Les capsules ont la plupart du temps un mode d’action sur une dizaine de mètres.
Les différents pièges commercialisés peuvent agir sur les mouches de la carotte, de la cerise et de l’olive, sur les carpocapses du poirier, du pommier et du prunier, sur les chenilles processionnaires du pin, sur les Teignes du poireau, sur les pyrales du maïs et les mineuses du marronnier.
La recherche
Actuellement, seules les phéromones sexuelles et les phéromones d’agrégation sont utilisées en agriculture. Mais certains chercheurs étudient l’utilisation des phéromones de pistes afin d’agir sur les futures invasions des fourmis d’Argentine.
Le réchauffement climatique fait craindre le pire aux scientifiques qui étudient les fourmis et plus particulièrement, les fourmis d’argentine. En effet, cela peut causer leur invasion. Ils étudient ainsi cette espèce invasive afin de pouvoir intervenir si une invasion se produit. Ils font l’expérience que nous avons décrite précédemment lors de l’étude des phéromones de piste, ils obtiennent les mêmes conclusions. Ils décident d’extraire la glande produisant les phéromones de piste et d’utiliser son contenu pour des besoins expérimentaux. Ainsi, ils tracent un nouveau parcours plus long que le précédent et y dépose la phéromone extraite afin de tracer une piste. Ils observent que les fourmis dévient de leurs chemins et suivent la piste tracée par les scientifiques. A long terme, ils veulent synthétiser ces phéromones et les diffuser dans une colonie. Les phéromones vont ainsi perturber la communication des fourmis. Dès lors, elles ne pourraient plus approvisionner correctement la fourmilière. Cette méthode pourrait ainsi aboutir à une diminution des fourmis d’Argentine (voir vidéo ci-dessous).
D’autre part, les entomologistes du centre INRA Bordeaux-Aquitaine ont réussi à diminuer le taux d’accouplement sans tuer un seul insecte. Ils ont utilisé la méthode de la confusion sexuelle dans les vignobles. Ils ont agi sur les Hétérocères en perturbant leur reproduction. En effet, ils ont montré que les femelles modifient leurs comportements et leurs succès reproducteurs lors de la diffusion de phéromones sexuelles.